服務熱線
18501696120
 更新時間:2025-10-31
更新時間:2025-10-31
 瀏覽次數:72次
瀏覽次數:72次
 更多推薦
更多推薦2025-11-04
2025-11-04
2025-11-04
2025-11-03
2025-11-03
2025-10-31
2025-10-31
2025-10-31
2025-10-30
2025-10-30

經皮給藥,這個被譽為 “無痛給藥革命" 的技術,一直以來被角質層這座 “天然屏障" 所束縛 —— 傳統認知中,只有分子量<500 Da、具備適度脂溶性的小分子才能穿透皮膚。而如今,一類被稱為 “離子液體" (ionic liquids,ILs)的特殊物質正在改寫這一規則:它能讓胰島素、siRNA 等水溶性大分子輕松穿越皮膚屏障,為外用制劑和經皮吸收制劑的開發開辟了全新賽道。
作為室溫下呈液態的有機鹽,離子液體憑借可調控的物理化學性質、優異的增溶能力和生物相容性,正從化學實驗室快步走進醫藥研發的重要舞臺。本文將系統解析離子液體在經皮給藥領域的技術突破、臨床進展及未來潛力,為制藥研發人員提供從基礎到應用的全景視角。
經皮給藥的優勢早已被行業認可:無需承受注射疼痛、規避肝臟首過效應、實現藥物長效緩釋…… 但皮膚最外層的角質層,由角質細胞與細胞間脂質緊密排列而成,如同 “銅墻鐵壁" 般阻斷了多數藥物的滲透。長期以來,能透過皮膚的藥物被死死限制在 “分子量<500 Da + 適度脂溶性" 的框架內,而當前醫藥研發的主力 —— 蛋白質、核酸、多肽等水溶性中大分子,幾乎被擋在門外,只能依賴注射給藥。
離子液體的出現,為這一困境帶來了轉機。這類由有機陽離子與有機 / 無機陰離子組成的液態鹽,通過調整離子組合可設計出無數種特性各異的溶劑。與水和有機溶劑相比,它不僅能顯著提升藥物的溶解度和穩定性,更能突破角質層屏障,讓原本無法透皮的藥物(即使是 hydrophilic macromolecules)順利滲透。
更重要的是,離子液體的 “多功能性" 使其成為經皮給藥的理想工具:既能作為溶劑溶解難溶性藥物,又能作為吸收促進劑打開皮膚通道,還能穩定易降解的生物制劑。這種 “一站式" 解決方案,讓它在止痛、抗炎、抗癌、糖尿病治療等多個領域展現出巨大潛力。

(ASCH VAPOSCAN經皮水分流失測量儀)

(Labodorf 850C皮膚角質量測試儀)
離子液體并非全新物質,但在醫藥領域的應用卻是近十年的突破。根據成分和特性,可分為 “舊世代" 和 “新世代" 兩大類,其安全性和適用性差異顯著。
早期研究中,咪唑鎓(imidazolium)、吡啶鎓(pyridinium)等陽離子,與四根(tetrafluoroborate)、六磷酸根(hexafluorophosphate)等含陰離子組成的離子液體是研究熱點。它們能有效改善藥物溶解性,但存在兩大短板:生物降解性差、毒性較高,且可能引發環境風險,限制了臨床應用。
為解決舊世代的缺陷,研究者將目光轉向生物相容性更高的成分,推動了新世代離子液體的誕生:
• 氨基酸基離子液體:Ohno 團隊以氨基酸為陰離子(如甘氨酸、丙氨酸),與 1 - 乙基 - 3 - 甲基咪唑鎓等陽離子結合,通過調整氨基酸側鏈和化學修飾,可調控粘性、玻璃化溫度等物性,生物相容性顯著提升。
• 膽堿基離子液體:Mitragotri 團隊開發的 CAGE(choline and geranic acid)是典型代表。由生物體內天然存在的膽堿(陽離子)和香葉酸(陰離子)組成,不僅安全性高,還自帶抗菌活性,已被廣泛用于多種藥物的經皮吸收研究。
• 醫用級離子液體庫(ILTS):MEDRx 株式會社建立的 ILTS 技術,精選已證實人體適用性的化合物組合,擁有 100-200 種離子液體庫,可根據藥物特性靈活選擇,兼顧高安全性和高效性。
新世代離子液體的另一大優勢是 “協同使用" 能力:可與水、油或微乳液復配,作為水層 / 油層成分增強藥物溶解。例如,Goto 團隊將離子液體與肉豆蔻酸異丙酯(油相)、吐溫 - 80(表面活性劑)組成 IL/O 微乳液,顯著提升了藥物的皮膚滲透性。
離子液體在經皮給藥中的價值,源于其在藥物溶解、穩定和透皮促進三方面的獨特作用,這些機制已被大量研究證實。
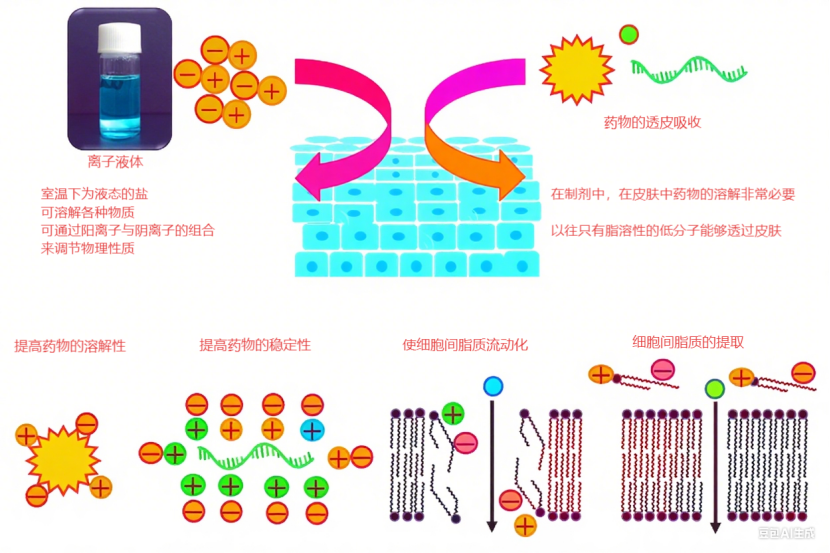
多數藥物(尤其是小分子化學藥)因水溶性差難以制成制劑,離子液體通過多種分子間相互作用解決這一問題:
• π-π 相互作用與氫鍵:含芳香環的藥物(如心血管藥 LASSBio-294)可與咪唑鎓陽離子的咪唑環形成 π-π 相互作用,同時與乙酸根等陰離子的氧原子形成氫鍵,溶解度顯著提升。
• 藥物離子液體化:將難溶性藥物直接轉化為離子液體是更有效的方案。例如,弱堿性藥物與脂溶性陰離子(如十二烷基硫酸根)結合后,可形成自組裝納米粒子,溶解度提升數十倍;弱酸性藥物托芬那酸(tolfenamic acid)與脂溶性陽離子(如丁基十二烷基二甲基銨)結合,也能通過類似機制增強溶解。
這種 “量身定制" 的溶解策略,讓許多 “躺平" 在實驗室的難溶性候選藥物重獲開發可能。
蛋白質、核酸等生物制劑易受溫度、酶、pH 影響而降解,離子液體的加入可顯著提升其穩定性:
• 保護核酸:siRNA 易被皮膚中的 RNase 降解,而膽堿 - 磷酸二氫根離子液體可通過濃度依賴方式抑制 RNase 活性,同時提高 siRNA 的融解溫度,增強熱穩定性。
• 穩定 DNA 與蛋白質:膽堿陽離子可與 DNA 骨架形成靜電相互作用,并與小溝(minor groove)產生疏水作用,維持 DNA 結構穩定;對于蛋白質,離子液體可抑制 pH、熱或振動引起的聚集和失活(如胰島素在特定離子液體中可減少聚集)。
這一特性讓離子液體成為 mRNA 疫苗、抗體藥物等生物制劑經皮給藥的 “保護傘"。
角質層的細胞間脂質和角蛋白是藥物透皮的主要障礙,離子液體通過多重機制突破這一屏障:
• 擾亂細胞間脂質:CAGE 等離子液體可抽出角質層中的脂質,同時增加其流動性,形成藥物滲透通道;1 - 辛基 - 3 - 甲基咪唑鎓離子液體的短烷基鏈可在脂質膜疏水區域制造空隙,提升通透性。
• 影響角蛋白:離子液體可改變角蛋白的排列結構,降低其對藥物的阻礙(如含離子液體的微乳液可擾亂角蛋白定向性)。
• 調節藥物 - 皮膚相互作用:部分離子液體可阻斷藥物與皮膚成分的結合(如 zaltoprofen 與神經酰胺的氫鍵),促進藥物在皮膚中的擴散。
這種 “多管齊下" 的促吸收機制,讓大分子藥物透皮從 “不可能" 變為 “常規操作"。
離子液體的臨床應用必須跨過 “安全性" 這道坎。其毒性與陽離子、陰離子的結構密切相關,需針對性評估:
咪唑鎓、吡啶鎓等陽離子的烷基鏈越長,與生物膜的相互作用越強,膜損傷風險越高。例如,長鏈烷基咪唑鎓對皮膚角質形成細胞的毒性顯著高于短鏈;而膽堿等天然來源的陽離子,毒性遠低于傳統咪唑鎓。
陰離子毒性整體較低,但脂溶性高或易水解的陰離子(如三氰基甲烷根、硫氰酸)毒性較高;而二甲磷酸根、根等陰離子對成纖維細胞的毒性較弱。
• CAGE:兼具抗菌活性和低皮膚刺激性,對細菌殺傷強但對正常細胞毒性低,已進入臨床研究。
• ILTS 技術:基于人體使用過的安全成分組合,毒性風險可控,相關貼劑已推進至臨床。
• 評估標準:皮膚應用需重點關注角質形成細胞毒性,建議結合三維皮膚模型等體外模型綜合評價。
通過優化離子組合(如縮短烷基鏈、選用天然來源離子),可在保證功效的同時將毒性降低。
離子液體經皮制劑的研發已從基礎研究邁向臨床,覆蓋多個疾病領域,部分產品已接近上市。
非甾體抗炎藥(NSAIDs)是經皮給藥的重點方向,離子液體的加入讓其效率和安全性更上一層樓:
• 依托度酸- 離子液體:依托度酸水溶性差,形成離子液體后,溶解度提升 80 倍,透皮量顯著增加,鎮痛抗炎效果更持久。
• 布洛芬 - 氨基酸離子液體:布洛芬與甘氨酸、丙氨酸形成的離子液體,水溶性提升 5 倍以上,透皮性增強且無明顯細胞毒性,適合長期外用。
皮膚疾病的局部給藥可減少全身副作用,離子液體讓藥物直達病灶:
• 特應性皮炎:STAT6 是誘發炎癥的重要因子,其誘餌 ODN(寡核苷酸)在 ILTS 技術輔助下透皮性提升 4 倍,可抑制 IL-4、IL-13 等炎癥因子,緩解皮膚肥厚。
• 銀屑病:NFKBIZ 是銀屑病惡化的驅動因子,將其 siRNA 溶于膽堿 - 香葉酸離子液體后,透皮量增加 5 倍,可降低 NFKBIZ 表達,減輕紅斑和角質細胞過度增殖。
• 皮膚感染:CAGE 不僅能促進頭孢他啶(ceftazidime)透皮,還可直接抑制生物膜形成,單獨或與抗生素聯用均能顯著增強抗菌活性。
皮膚相關癌癥(如黑色素瘤)或體表腫瘤可通過離子液體經皮給藥實現局部高濃度治療:
• 黑色素瘤:BCL-2 抑制劑 navitoclax 在膽堿 - 辛酸離子液體中溶解度提升 150 倍,雖透皮總量略低,但真皮中藥物濃度更高,腫瘤局部療效增強且全身毒性降低。
• 癌癥疫苗:OVA 肽、WT1 肽等腫瘤抗原在離子液體輔助下可高效透皮,激活皮膚中的抗原呈遞細胞,誘導特異性 CD8+ T 細胞應答,抑制肺癌等腫瘤生長(如 ILTS 制劑可同時促進肽抗原和佐劑 resiquimod 吸收,增強免疫應答)。
胰島素等多肽藥物的經皮給藥是糖尿病患者的福音:
• 胰島素經皮制劑:胰島素溶于 CAGE 后可保持二級結構,透皮后 4 小時內血糖降低 40%,作用持續 12 小時,有望替代部分注射制劑。
• 諾比列汀(nobiletin)透皮:作為黃酮類降糖藥,nobiletin 在 CAGE 中透皮性增強,可實現長期平穩降糖,適合 2 型糖尿病管理。
目前,離子液體經皮制劑的臨床轉化已取得階段性成果:
• MEDRx 公司:帶狀皰疹后神經痛治療貼劑 Lydolyte 已完成臨床,2023 年 3 月提交上市申請;替扎尼定(痙攣麻痹)、(鎮痛)貼劑進入臨床。
• CAGE Bio 公司:CAGE 為主成分的 CGB400 治療酒渣鼻樣皮炎的臨床研究正在推進。
未來,隨著 AMED 等機構對 “中分子藥物經皮 / 經腸吸收促進技術" 的投入,離子液體的應用將從經皮擴展到更多給藥途徑。同時,新型離子液體的設計(如響應性智能離子液體)、聯合其他促透技術(如微針、電穿孔)或將進一步突破現有瓶頸。
對于制藥研發人員而言,離子液體的價值不僅在于 “解決問題",更在于 “創造可能"—— 它讓原本因給藥限制被放棄的候選藥物重獲生機,讓復雜制劑的開發變得更簡單高效。或許在不久的將來,“一抹就好" 的胰島素、“一貼抗癌" 的靶向藥,將成為臨床常態。
離子液體在經皮給藥領域的崛起, “材料創新" 推動 “制劑革命" 。從突破角質層屏障到穩定生物制劑,從實驗室的分子設計到臨床的貼劑應用,它正一步步改寫經皮給藥的 “規則手冊"。對于制藥研發人員而言,把握離子液體的特性與應用邏輯,或將在新一輪制劑創新浪潮中搶占先機。未來已來,離子液體與經皮給藥的結合,終將為患者帶來更安全、更便捷、更有效的治療選擇。
參考文獻
1)Taro Shimizu, Hidetoshi Hamamoto, Tatsuhiro Ishida, Development and medical application of ionic liquid-based transdermal formulations, Drug Delivery System, 2023, Volume 38, Issue 3, Pages 230-238,
2)Gomes, J.M., et al., Chem. Soc. Rev., 48, 4317-4335(2019)
3)Ohno, H., et al., Acc Chem. Res., 40, 1122-1129(2007)
4)Fukumoto, K., et al., J. Am. Chem. Soc., 127, 2398-2399(2005)
 返回列表
返回列表